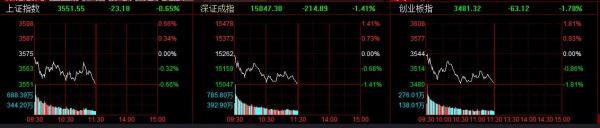
辉瑞新冠口服药授权国内仿制,这些企业入围!国内研发进展如何?
5家中国企业与MPP签署协议,获准生产辉瑞的新冠治疗口服药,其中有4家A股上市公司与此同时,国内药企也在加紧研发新冠治疗口服药
3月17日晚间,药品专利池组织正式公开宣布,与包括中国复星医药在内的全球35家企业签订协议,授权其生产辉瑞口服新冠治疗药物奈玛特韦仿制药。
在本次与MPP签署协议的35家企业中,共有5家中国企业,分别是上海迪赛诺,华海药业,普洛药业,复星医药,九洲药业其中,九洲药业获授权生产原料药,另外4家可同时生产原料药和制剂
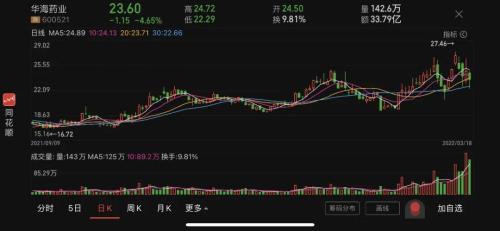
日前,5家药企中的4家A股上市公司股价涨跌不一华海药业股价报收23.6元/股,跌幅为4.65%,普洛药业报收33.56元/股,涨幅为0.21%,复星医药A股报收50.47元/股,涨幅为2.54%,九洲药业报收46.85元/股,跌幅为4.41%
全球市场规模或达百亿美元
Paxlovid是一种口服的小分子新冠治疗药物,由奈玛特韦和少剂量的利托那韦两种核心成分构成。
奈玛特韦作为其中的主要成分,能抑制新冠病毒与人体结合,利托那韦则能延长奈玛特韦的药效。
在实际生产过程中,两种成分可由不同厂家分别生产,最后完成组装。简单来说,两种药物的相关实验数据都不完整,且尚未在经同行审评的专业期刊发表。
目前,Paxlovid的产能仍有较大缺口根据消息显示,辉瑞已将2022年Paxlovid的产量预计提高到1.2亿疗程,并计划今年在美国交付2000万疗程,但据其预期,2022年全球大约有2.5亿人需要抗病毒药物,即约有1.3亿疗程缺口
而据相关媒体报道,针对辉瑞Paxlovid,美国,英国,日本已分别累计采购2000万,275万,200万疗程,针对默沙东Molnupiravir,美国,英国,日本已分别累计采购950万,230万和160万疗程。。
由此,天风证券分析指出,未来伴随着Paxlovid的全球范围获批与MPP协议的全球销售,相关供应链订单需求量可观且有望保持扩张。
另外,西南证券预计,全球口服新冠药物市场规模为数十亿至上百亿美元2021年全球新增新冠患者约为1.8亿人,假设口服药物每疗程单价分别为500/300/100美元,对应市场空间分别为900/540/180亿美元当前全球患病率为0.31%,若患病率下降到0.15%或者上升到0.45%,则对应市场规模分别为450/270/90亿美元,1350/810/270亿美元
同时,华创证券研报认为,预计欧美发达国家市场在300亿美元级别,国内相关CMO供应链业务有望持续拓展此外,国产新冠口服药未来每年需求量有望达到亿人份级别
对药企业绩影响尚难预测
通过MMP与研发药企的谈判,根据自愿,可以达成将其药品专利放入专利池的协议当仿制药企向MPP申请获得专利实施许可后,便可生产药品以低价向特定的低收入国家患者提供不过,中国并不在MPP划定的中低收入国家之列
需要注意的是,这并非中国药企首次获得授权仿制新冠口服药。
虽然产能需求较大,但根据目前华海药业,复星医药和此前入选企业发布的风险提示来看,对公司业绩的影响或许并没有这么简单。
日前,华海药业与复星医药双双发布公告。
华海药业提到,鉴于本次合作旨在帮助95个国家可负担地获取许可产品,相关定价预计将低于原研产品或在其他中高收入国家的售价截至目前,该许可产品的具体成本和定价等暂无法确定,对公司未来业绩影响尚无法预计
同时复星医药也表示,许可产品于区域内上市后的销售情况受新冠疫情发展,生产及供应链能力,市场竞争环境,销售渠道等诸多因素影响,存在不确定性截至本公告日,公司尚无在手订单,也尚未开展正式生产
而在今年1月,默沙东新冠口服药授权国内仿制后,就有分析人士称,这或许是一场免费的公益行动更有部分业内人士认为,此次获得仿制药授权主要供给中低收入国家,偏公益属性,给公司带来的利润空间有限
新冠口服药何时上市
日前,据中国香港特别行政区政府公报,首批新冠口服抗病毒药物Paxlovid已于3月14日运抵香港,并于当日送往医院管理局使用。默克和辉瑞提供的均为Ⅲ期临床试验中期分析数据,这是一项药物试验在经受安全检测时判定是否继续下去的节点。
在国内,据上海海关最新消息,3月17日晚间,2.12万盒进口抗新冠病毒药物奈玛特韦片/利托那韦片,经上海外高桥保税区海关验放,办结全部进口通关手续后,迅速运往全国抗疫一线这是该药物被纳入最新版新冠肺炎诊疗方案后的全国首批进口产品
日前,国家药监局根据药品管理法相关规定,按照药品特别审批程序,进行应急审评审批,附条件批准辉瑞公司新冠病毒治疗药物Paxlovid进口注册。
后在3月15日,据国家卫健委发布的《新型冠状病毒肺炎诊疗方案》修订要点显示,Paxlovid特异性抗新冠病毒药物被写入诊疗方案。
除了辉瑞,国内药企也加快了新冠口服药的研发进度根据消息显示,新冠口服药适用于新冠检测阳性的高危人群,能够帮助潜在高危患者避免新冠重症目前我国已投入约3.15亿元研发各类治疗新冠的药物,已立项药物约有53个
据华创研究研报显示,真实生物的阿兹夫定处于临床Ⅲ期阶段,君实生物/旺山旺水/中科院的VV116已启动临床II/III期研究,歌礼制药,先声药业,众生药业,君实生物等公司的口服3CL抑制剂处于临床前研究阶段,有望在未来6个月陆续进入临床。
。声明:本网转发此文章,旨在为读者提供更多信息资讯,所涉内容不构成投资、消费建议。文章事实如有疑问,请与有关方核实,文章观点非本网观点,仅供读者参考。
猜您喜欢